Giải bài tập hóa 10 sgk trang 83
Có thể bạn quan tâm
[bài 17 hóa học lớp 10] giải bài 1, 2 trang 82; bài 3, 4, 5, 6, 7, 8 trang 83 SGK Hóa Học 10: Phản ứng oxi hóa – khử – Chương 4
Bạn Đang Xem: Bài 1,2,3, 4,5,6,7,8 trang 82,83 SGK Hóa 10: Phản ứng oxi hóa – khử
i- Định nghĩa sự oxi hóa – Xác định phản ứng khử và số oxi hóa
1. Định nghĩa phản ứng oxi hóa khử
Phản ứng oxi hóa khử là phản ứng hóa học trong đó số oxi hóa của một số nguyên tố thay đổi, hoặc phản ứng oxi hóa khử là phản ứng trong đó các electron được chuyển giữa các chất phản ứng. .
2. Xác định số oxi hóa trong hợp chất
Chú ý: Người ta viết số oxi hóa phía trên nguyên tử nguyên tố. Đánh dấu trước, sau đó đánh số.
Hai. Mối quan hệ giữa hóa trị của nguyên tố và số oxi hóa
Chúng ta biết rằng một số nguyên tố có nhiều hóa trị khác nhau, vậy có mối quan hệ nào giữa số oxi hóa của một nguyên tố và hóa trị của nó không?
Hóa trị liên quan đến liên kết hóa học. Số oxi hóa liên quan đến sự chuyển electron nên đôi khi số oxi hóa không tương ứng với hóa trị.
Trong nhiều trường hợp, đặc biệt là các hợp chất kim loại, giá trị tuyệt đối của số oxi hóa và hóa trị thường giống nhau.
iii- chất khử, chất oxi hóa, chất oxi hóa, chất khử
- Chất khử là chất nhường electron hoặc tăng số oxi hóa sau phản ứng.
- Chất oxi hóa là chất nhận electron hoặc chất có số oxi hóa bị giảm sau phản ứng.
- Sự oxi hóa một chất là làm cho chất đó mất electron hoặc tăng số oxi hóa của nó.
- Tính khử của một chất là làm cho chất đó nhận electron hoặc giảm số oxi hóa của chất đó.
Quyên góp điện tử chỉ xảy ra khi thu được điện tử. Vậy sự oxi hóa và sự khử luôn xảy ra đồng thời trong một phản ứng.
iv- 0 phương trình phản ứng oxi hóa – khử
Để lập phương trình phản ứng oxi hóa khử bằng phương pháp mặt trăng electron, chúng ta thực hiện các bước sau:
Bước đầu tiên: viết số oxi hóa của nguyên tố có số oxi hóa thay đổi:
Bước thứ hai: viết quá trình oxi hóa khử và cân bằng từng quá trình:
Bước 3: tìm hệ số thích hợp sao cho tổng số electron do chất khử nhường bằng tổng số electron do chất oxi hóa nhận
Đáp án và lời giải chi tiết bài 82, 83 trang 10 Bài 17 Hóa học: Phản ứng oxi hóa – khử
bài đăng 1.Trả lời:
A. 2hgo -tº→ 2hg + o2
Xem Thêm: Cách tính cung mệnh theo năm sinh. Bảng tổng hợp tra cứu cung mệnh
СаСОз -tº→ cao + khí cacbonic.
2al(oh)3 -tº→ al2o3 + 3h2o
2nahco3 -tº→ na2co3 + co2 + h2o
Phản ứng nào là phản ứng oxi hóa khử.
Đáp án đúng: 2hgo -tº→ 2hg + o2
Xem Thêm : Đoạn Văn Tiếng Anh Hay Về Cuộc Sống
bài 2.Trả lời:
A. 4nh3 + 5o2 —> 4 giờ + 6 giờ 2 giờ
2nh3 + 3cl2 —> n2+6hcl
nh3 + 3cuo —> 3cu + n2 + 3h2o
2nh3 + h2o2 + mns04 —> mn02 + (nh4)2so4.
Trong phản ứng nào nh3 không đóng vai trò là chất khử?
Đáp án đúng: d.2nh3 + h2o2 + mns04 —> mn02 + (nh4)2so4.
Bài 3 trang 83 Hóa học 10:Các phản ứng sau:
A. hno3 + nah → nano3 + h2o
n2o5+ h2o → 2hno3
2hno3 + 3h2s → 3s + 2no + 4h2o
2fe(oh)3 → fe2o3 + 3h2o.
Phản ứng nào là phản ứng oxi hóa khử.
Xem Thêm: Bếp lửa (Tự học có hướng dẫn)
Giải thích: Trong số các phản ứng trên, chỉ có phản ứng c là phản ứng oxi hóa khử, vì số oxi hóa của nguyên tố đã thay đổi.
bài 4.Đáp án: 3no2 + h2o → 2hno3 + không
Vai trò của no2?
A. Chỉ là một chất oxi hóa.
Chỉ là chất khử.
Vừa là chất oxi hóa, vừa là chất khử.
Không phải chất oxi hóa, không phải chất khử
Chọn câu trả lời đúng
Giải thích: no2 vừa là chất oxi hóa, vừa là chất khử: c đúng.
Bài 5 trang 83: Phân biệt chất oxi hóa và chất oxi hóa, chất khử và chất khử. Ví dụ.
Hướng dẫn bài 5: Chất oxi hóa là chất nhận electron.
Sự oxi hóa một chất là sự nhường electron của chất đó.
Xem Thêm : Hé lộ ý nghĩa tên Thanh Thảo – Tên Thanh Thảo có tốt không?
Chất khử là chất cho electron.
Sự khử của vật chất là sự nhận electron.
Ví dụ: fe + cuso4 → feso4 + cu
– Nguyên tử Fe nhường electron, là chất khử. Fe bị mất electron gọi là quá trình oxi hóa nguyên tử sắt.
– Ion đồng nhận electron và là chất oxi hóa. Ion đồng nhận electron gọi là sự khử ion đồng.
Bài 6: Phản ứng oxi hóa khử là gì? Cho ba ví dụ.
Xem Thêm: 50 Hình nền điện thoại độc đáo, chất nhất
Hướng dẫn: Phản ứng oxi hóa khử là phản ứng hóa học trong đó các electron được chuyển giữa các chất phản ứng.
Ví dụ:
bài 7.Theo phương pháp cân bằng điện tử, lập phương trình phản ứng oxi hóa khử sau:
a) Dùng dung dịch axit clohiđric đặc phản ứng với mncl2 tạo ra mncl2, cl2 và h2o.
b) Phản ứng với axit nitric đặc nóng tạo thành cu(no3)2, no2 và h2o.
c) mg phản ứng với axit sunfuric đặc nóng thu được mgso4, s và h2o.
Giải 7:Phương trình phản ứng oxi hóa khử:
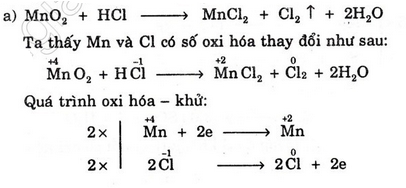
 b)
b)

c)

Bài 8. ( sgk hóa học 10 tr 83) Cần bao nhiêu gam đồng để khử hoàn toàn lượng ion bạc có trong 85 ml dung dịch agno3 0,15M?
Đọc Bài 8:
Phương trình hóa học của phản ứng:
cu + 2agno3 -> cu(no3)2 + 2ag
1mol 2mol
x nốt ruồi 0,01275 nốt ruồi
x = 0,01275 / 2 = 0,06375 nốt ruồi
Mcu tham gia phản ứng: 0,006375 x 64 = 0,408 g.
Nguồn: https://anhvufood.vn
Danh mục: Giáo Dục




