Có thể bạn quan tâm
- Bài viết số 2 lớp 8 đề 2: Kể về một lần em mắc khuyết điểm khiến thầy (cô) giáo buồn 2 Dàn ý & 19 mẫu bài viết số 2 lớp 8 đề 2
- 10 câu chuyện ngắn và 10 bài học sâu sắc giúp bạn sống ý nghĩa hơn
- Văn mẫu 8 Người ấy sống mãi trong lòng tôi về mẹ hay nhất
- Hướng dẫn tách nền ảnh trên điện thoại đơn giản bằng PicsArt
- Cảm nhận về bài thơ Thương vợ – Tú Xương | Văn mẫu 11
Bảng tuần hoàn hóa học cấp 8 là bảng tuần hoàn đơn giản nhất chỉ có 30 nguyên tố phổ biến nhất trên tổng số 118 nguyên tố. Nó ở trang 42 ở đầu Chương 2. Bảng tuần hoàn các nguyên tố hóa trị 8 bậc chỉ bao gồm những thông số đơn giản nhất như số proton, tên nguyên tố, ký hiệu hóa học, nguyên tử khối, hóa trị. Dễ vì học sinh mới bắt đầu làm quen với hóa học. Hóa trị liên quan đến cách bạn viết phương trình phản ứng hóa học, vì vậy hãy ghi nhớ số hóa trị
Bạn Đang Xem: Bảng tuần hoàn hóa học lớp 8 trang 42
Bạn sẽ sử dụng bảng tuần hoàn này nhiều lần vì trong bài 45 lớp 8 chúng ta sẽ phải xem lại bảng tuần hoàn ở trang 48. Tôi đã liệt kê chúng dưới đây để thuận tiện cho bạn khi bạn học ở nhà hoặc không có sách giáo khoa.
Bảng tuần hoàn cấp 8 Trang 42
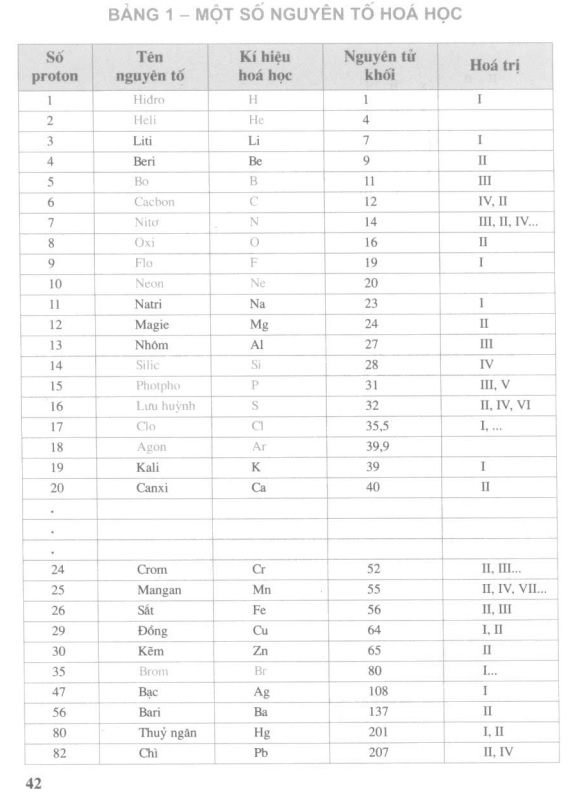
Cơ sở thực tế của bảng tuần hoàn các nguyên tố bậc 8
Bảng tuần hoàn các nguyên tố mà chúng ta sử dụng ngày nay dựa trên bảng do Dmitri Mendeleev phát minh và xuất bản năm 1869.
Xem Thêm: 20 mẫu hình xăm xương rồng đẹp và ý nghĩa đằng sau chúng – Owl Ink Studio – Xăm Hình Nghệ Thuật
Mendeleev nhận thấy rằng ông có thể sắp xếp 65 phần tử đã biết vào một bảng sao cho mỗi phần tử có:
Xem Thêm : Biểu diễn hình học của số phức là gì? Công thức và cách dạng bài tập
1.Khối lượng nguyên tử lớn hơn khối lượng của nguyên tố bên trái nó. Ví dụ, magie (trọng lượng nguyên tử 24,3) nằm bên phải natri (trọng lượng nguyên tử 23,0).
Năm 1913, hóa học và vật lý bắt đầu lẫn lộn. Một số nhà khoa học hàng đầu, bao gồm cả Mendeleev, đã nói một cách nghiêm túc về các nguyên tố nhẹ hơn hydro và các nguyên tố nằm giữa hydro và heli. Tạo ra tầm nhìn về nguyên tử và bằng chứng của Mendeleev về bảng tuần hoàn các nguyên tố dựa trên trọng lượng nguyên tử.
2.Tính chất hóa học của cùng một cột là như nhau. Hay nói cách khác, cùng một chất hóa học. Ví dụ, magiê rơi vào cột kiềm thổ cùng với các nguyên tố khác có phản ứng tương tự.
Mendeleev nhận ra rằng bảng tuần hoàn sẽ trở thành tâm điểm của hóa học. Ngoài ra, Mendeleev phát hiện ra rằng bảng tuần hoàn của ông không đầy đủ và dự đoán những khoảng trống và tính chất phải có của các nguyên tố còn thiếu trong bảng tuần hoàn trong tương lai.
Xem Thêm: Các thao tác lập luận trong văn nghị luận
Cũng giống như Adams và Le Verrier có thể được coi là đã phát hiện ra Sao Hải Vương trên giấy tờ. Mendeleev được ghi nhận là người đã khám phá ra gecmani trên giấy. Ông đặt tên cho nguyên tố mới là eka-silicon sau khi quan sát khoảng cách giữa silicon và thiếc trong bảng tuần hoàn:
Tương tự, Mendeleev cũng phát hiện ra gali (eka-nhôm) và scandi (eka-boron) trên lý thuyết. Bởi vì ông đã dự đoán sự tồn tại và tính chất của chúng trước khi chúng thực sự được phát hiện.
Xem Thêm : Đây là cách viết số mũ trong Word đơn giản có thể bạn chưa biết
Mặc dù đã tạo ra bước đột phá quan trọng nhưng Mendeleev vẫn có những suy luận sai lầm. Mendeleev tin rằng tính chất hóa học được xác định bởi trọng lượng nguyên tử. Tất nhiên, nó có ý nghĩa hoàn hảo với hóa chất vào thời điểm đó.
27 năm sau khi xuất hiện bảng tuần hoàn các nguyên tố đầu tiên, electron với đã được phát hiện. Và phải mất 44 năm để tìm ra lời giải thích chính xác về tính chất của bảng tuần hoàn Mendeleev…
Hóa học lớp 8 chúng ta sẽ học những gì
Xem Thêm: Bức tranh thiên nhiên trong Đoàn thuyền đánh cá (9 mẫu) – Văn 9
Chúng ta sẽ bắt đầu học hóa học lớp 8 và làm quen với bảng tuần hoàn các nguyên tố hóa học. Vì hóa học rất phức tạp và khó hình dung nên ở lớp 7 không dạy.
Khi bắt đầu học hóa học lớp 8, chúng ta sẽ bắt đầu làm quen với những khái niệm hóa học cơ bản nhất và các dụng cụ thí nghiệm. Những kiến thức cơ bản về hóa học ở lớp 8 rất quan trọng vì nó là nền tảng mà bạn sẽ học tập chăm chỉ trong vài năm tới. Vì vậy cần lưu ý rằng hóa học là một trong những môn học rất quan trọng sau này vì nó thường xuất hiện trong các kỳ thi tuyển sinh cấp 3 trở lên và đại học.
Kiến thức chung hóa học lớp 8 là:
Bài 1: Nhập môn Hóa học
Chương 1: Vật chất-Nguyên tử-Phân tử
- Bản nhạc 2: Chất
- Bài 3: Bài tập 1
- Bài 4: Nguyên tử
- Bài 5: Nguyên tố hóa học
- Bài 6: Nguyên tố và hợp chất – Phân tử
- Bài 7: Bài thực hành 2
- Bài 8: Bài tập 1
- Bài 9: Công Thức Hóa Học
- Bài 10: Hóa trị
- Bài 11: Bài thực hành 2
- Bài 12: Phép biến hình
- Bài 13: Phản ứng hóa học
- Bài 14: Bài tập 3
- Bài 15: Định luật bảo toàn khối lượng
- Bài 16: Phương Trình Hóa Học
- Bài 17: Bài tập 3
- Quỹ đạo 18: Moore
- Bài 19: Chuyển đổi giữa Khối lượng, Thể tích và Số lượng
- Bài 20: Khối lượng riêng của chất khí
- Bài 21: Công Thức Hóa Học
- Bài 22: Tính từ phương trình hóa học.
- Bài 23: Bài tập 4
- Bài 24: Tính chất của Oxy
- Bài 25: Sự oxi hóa – Phản ứng hóa học – Ứng dụng của oxi
- Trở về 26: Oxit
- Bài 27: Phản ứng tạo oxi – phân hủy
- Bài 28: Không khí – Lửa
- Bài 29: Bài tập 5
- Bài 30: Bài thực hành 4
- Điều 31: Tính chất – Ứng dụng của Hiđro
- bài 32: Phản ứng oxi hóa – khử
- Bài 33: Điều chế khí hiđro – Phản ứng thế
- Bài 34: Bài thực hành 6
- Bài 35: Bài tập 5
- Bài 36: Nước
- Bài 37: Axit – Bazơ – Muối
- Bài 38: Luyện tập bài 7
- Bài 39: Bài thực hành 6
- Sau 40: Giải pháp
- Bài 41: Sự tan của các chất trong nước
- Bài 42: Nồng độ dung dịch
- Bài 43: Phát triển giải pháp
- Bài 44: Luyện tập Bài tập 8
- Bài 45: Bài thực hành 7
- 5 cách nhanh nhất để ghi nhớ bảng tuần hoàn
Chương 2: Phản ứng hóa học
Chương 3: Nốt ruồi và hóa học
Chương 4: Oxy – Không khí
Chương 5: Hydro – Nước
Chương 6: Giải pháp
Có thể thấy, kiến thức hóa học lớp 8 chỉ bao gồm những kiến thức đơn giản. Nhưng nó cũng khá nặng, với 45 bài trong 6 chương. Nếu bạn không muốn mất nền tảng của những môn học quan trọng nhất ở trường cấp hai và cấp ba, tôi khuyên bạn nên tập trung.
Bài viết liên quan:
Nguồn: https://anhvufood.vn
Danh mục: Giáo Dục
- 20 mẫu hình xăm xương rồng đẹp và ý nghĩa đằng sau chúng – Owl Ink Studio – Xăm Hình Nghệ Thuật
- Cách nấu canh kim chi thịt heo ngon chuẩn vị Hàn, ai ăn cũng mê
- TẢI 101+ hình ảnh cuộc sống bình yên đẹp giúp tâm thanh tịnh
- My Talking Tom Hack APK Full Tiền Vàng Kim Cương Max level 999
- Cách nấu cháo chim bồ câu ngon, bổ dưỡng, không tanh




